注意缺陷与多动症(专业版)
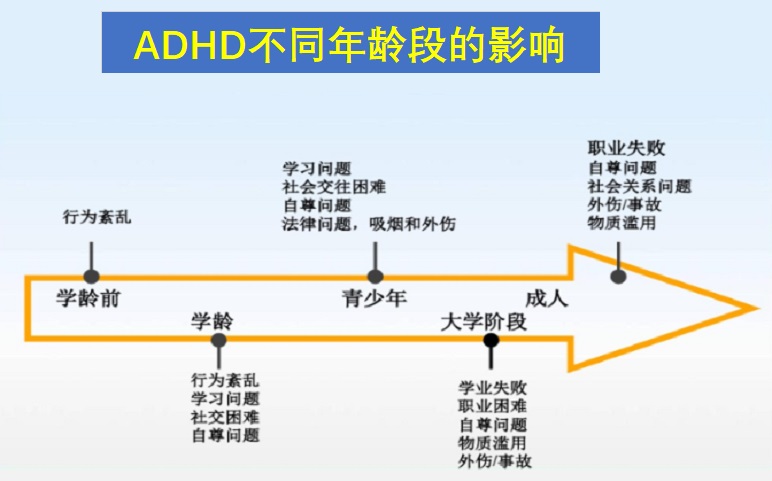
注意缺陷多动障碍(ADHD)是一种疾病,影响人的行为。它可引起多动、冲动的行为和/或难以集中注意力。
其他名称:注意力缺陷障碍;多动症;多动冲动障碍
英文名称:Attention Deficit Hyperactivity Disorder and Attention Deficit Disorder,ADHD and ADD; Hyperkinetic Syndrome; Hyperkinetic Impulse Disorder
ADHD有3种类型:
症状根据ADHD的类型而不同:
调整饮食与生活方式
越来越多的研究表明饮食变化可以显着改善ADHD症状:
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控ADHD的营养和草本补充剂,主要包括如下:
1.维生素和矿物质类:
1.1.复合维矿素等多种营养素:
1.2.维生素B族:
B族维生素是一类水溶性营养素,在新陈代谢和维持体内平衡方面发挥着至关重要的作用。已发现患有ADHD儿童和成人的B族维生素,即维生素B6(吡哆醇)和叶酸(B9)水平降低;此外,发现患有多动症的儿童的维生素B12(钴胺素)水平显著低于对照组6,7,。B族维生素缺乏可能会导致疾病病理,因为它们在血清素、儿茶酚胺和其他单胺类的产生中起着重要作用。
B族维生素也因其降低血液同型半胱氨酸水平的能力而备受关注,因为在包括ADHD在内的多种疾病中都观察到高水平的同型半胱氨酸,并可能导致氧化应激8-10。需要进一步的研究来阐明B族维生素和同型半胱氨酸在ADHD病理中的关系。
1.3.维生素B6和镁:
维生素B6(吡哆醇)与血清素的产生有关。早期研究发现,补充B6可以提高血清素水平,改善ADHD的多动症状11。在一项营养调查中,将100名ADHD患者与150名健康人进行了比较,发现ADHD患者的维生素B6摄入水平明显较低。研究还表明,镁缺乏症在多动症患者中很常见12,13。在一项安慰剂对照试验中,每天补充约200mg镁,持续六个月,显示7-12岁ADHD儿童的多动症状显著减少14。
一项针对40名ADHD儿童的为期8周的研究发现,补充镁(6mg/kg/天)和维生素B6(0.6mg/kg/天)可以改善多动症和学校注意力。有趣的是,当停止治疗方案时,儿童的症状在几周内再次出现15。在同一研究人员之前的一项研究中,类似的维生素B6和镁补充剂方案改善了过度兴奋症状。在这项研究中,52名过度兴奋的儿童服用了镁-B6补充剂,为期6个月;在治疗期间,所有受试者的身体攻击性和注意力等症状都有所改善16。
1.4.锌:
锌参与多巴胺能信号传导,已被证明是ADHD患者常见的营养缺乏症17,18。与接受利他林和安慰剂治疗的儿童相比,接受利他林治疗六周的多动症儿童在同时服用锌补充剂(每天55mg硫酸锌,提供15mg元素锌)时,从老师和家长那里获得了更好的行为评价19。
在一项针对400名ADHD儿童(平均年龄9.6岁)的大型研究中,作为单一疗法,每天150mg硫酸锌持续12周,与安慰剂相比,可显著改善多动、冲动和社交障碍症状20。
1.5.铁:
铁是身体中的一种重要微量元素,对生长、发育、红细胞氧气输送和多巴胺信号传导很重要21。铁以铁蛋白储存在体内,铁蛋白随后可以按照身体的要求以可控的方式释放铁22。在ADHD患者中观察到低铁蛋白水平,提示铁蛋白在多动症病理中的重要作用23,24。许多患有多动症的儿童都是缺铁性的,缺铁的严重程度与症状的严重程度相关25。在患有ADHD和睡眠障碍(如不安腿综合征)的儿童中也观察到低铁水平23,21。
一项针对23名患有ADHD和缺铁(定义为铁蛋白水平低于30ng/mL)的儿童(5-8岁)的随机安慰剂对照研究表明,在12周内每天补充80mg硫酸亚铁(提供16mg元素铁)可显著降低症状26。另一项针对14名受试者(7-11岁)的试验表明,每天补充5mg/kg持续30天,显著降低了父母对ADHD症状的评分27。在一项对52名服用哌甲酯的缺铁儿童进行的试验中,随机接受补铁(含80mg元素铁的300mg硫酸亚铁胶囊)或安慰剂12周,父母报告接受铁治疗的儿童ADHD症状有显著改善,但接受安慰剂治疗的人则没有28。
需要注意的是,超过膳食推荐量(RDA)的高剂量铁(如这些试验中使用的铁)只能在医疗从业者的指导下使用,因为意外过量服用含铁产品是6岁以下儿童致命中毒的主要原因。
1.6.维生素D:
维生素D是一种脂溶性维生素,通过饮食获得,并由身体在阳光照射下合成。维生素D缺乏被认为是几种神经精神障碍的可能原因,也可能是ADHD的危险因素。一项对8项共11,324名儿童(2655名患有多动症)的研究进行的荟萃分析发现,与健康对照组相比,被诊断为ADHD
的患者的维生素D血清水平显著较低29。在一项对5项研究进行的另一项荟萃分析中,维生素D状态较低与患ADHD的风险较高显著相关30。维生素D缺乏也可能导致情绪障碍,通常与ADHD共存31。
补充维生素D已在各种临床试验中被用作改善ADHD症状的治疗方法。一项双盲试验将54名儿童(5-12岁)随机分组,接受2000 IU(50mcg)维生素D或安慰剂治疗8周,作为哌甲酯的辅助治疗。虽然ADHD症状在两组中均显著降低,每周通过父母晚间和早晨行为评分(WPREMB)标准化评估观察到的晚间症状,在服用维生素D的第4周和第8周得到改善32。在一项单独的试验中,包括96名患有ADHD的儿童,随机接受每周50,000 IU(1250mcg)的维生素D或安慰剂治疗六周(以及稳定的每日剂量的哌甲酯),维生素D组的多动症症状有所改善,对注意力不集中症状有特别的影响33。此外,一项包含256名儿童的四项随机对照试验的系统回顾和荟萃分析发现,维生素D补充剂在ADHD总分、注意力不集中评分、多动评分和行为评分方面显示出虽小但在统计学上显著的改善34。
一项医院研究实例:ADHD管理的多种营养配方
ADHD的多因素起源表明,针对多种特定潜在促成因素的干预可能是有益的。为了验证这一假设,美国马萨诸塞州McLean医院的研究人员将20名患有ADHD的儿童分为两组。一组10名儿童每天服用5-15mg利他林2-3次,另一组接受综合性多营养配方,该配方旨在针对可能在ADHD发展中发挥作用的几个因素35。
本研究中使用的多种营养配方包括益生菌、氨基酸(如酪氨酸、组氨酸、谷氨酰胺、甘氨酸、蛋氨酸和半胱氨酸)、必需脂肪酸和磷脂(如EPA、DHA和磷脂酰胆碱)以及维生素和矿物质。
令人印象深刻的是,在标准化ADHD评估中,服用多种营养配方的儿童在4周时的ADHD症状改善程度与服用利他林的儿童相同。在结束研究时,研究人员指出:“两组的进步……都是显著的,基本上是相同的……”
2.必需脂肪酸:
研究发现,患有ADHD的儿童血液中的ω-3脂肪酸水平可能较低36。虽然现代饮食通常含有过多的某些ω-6脂肪酸,但缺乏ω-3脂肪酸类(包括EPA和DHA)37,38。考虑到产生多巴胺的神经末梢由高达80%的ω-3脂酸DHA组成39,这些分子在中枢神经系统及其功能中具有重要作用。在儿童中,ADHD症状的严重程度与较低水平的ω-3和较高水平的ω-6脂肪酸有关。一般来说,多动和注意力不集中也与ω-3脂肪酸缺乏有关,因此表明这可能是ADHD的一个风险因素40。
英国一项针对493名7-9岁学龄儿童的研究发现,ω-3脂肪酸缺乏非常常见,并与ADHD相关症状(如对立行为和情绪不稳定)有关。另一组研究发现,血液中ω-3脂肪酸水平低与冷酷无情的行为、反社会特征和情绪处理受损有关41,42。
瑞典科学家研究了鱼油补充剂对75名患有多动症的儿童和青少年的影响,这些鱼油补充剂含有ω-3脂肪酸(每天558mg EPA, 174mg DHA)和有益的ω-6脂肪酸亚麻酸GLA(60mg/天)。他们发现,六个月后,近一半的受试者对ω-3和ω-6补充剂有反应,ADHD症状减轻43。在随后对这些研究数据的分析中,同样的研究人员发现,症状减轻至少25%的受试者在三个月和六个月时,血液中ω-6与ω-3的比例显著降低44。
耶鲁大学研究人员进行的一项全面审查,回顾了涉及699名ADHD儿童的10项试验的证据。研究发现,补充ω-3脂肪酸可以适度改善研究参与者的ADHD症状。研究人员在总结中指出,“……使用ω-3脂肪补充剂来加强传统的药物干预可能是合理的……”45。对几项已发表研究的分析还发现,补充游离脂肪酸和从饮食中排除人工食用色素,在减少ADHD症状方面具有统计学上的显著效果46。
亚麻籽油提供高水平的ω-3脂肪酸α-亚麻酸(ALA),这是EPA和DHA的前体,也可能有益。一项研究考察了每天两次给患有ADHD的儿童补充亚麻油乳剂(提供200mg ALA)和维生素C乳剂(25mg)的益处,发现ADHD的症状显著改善,包括冲动、烦躁、注意力不集中和自我控制,这反映在多动症总分的降低上47。
鱼油是多不饱和ω-3脂肪酸的良好来源。脂肪酸水平的平衡可以通过血液测试来测量,服用脂肪酸补充剂的人可以重复进行血液测试来衡量其效果。
3.丝氨酸磷脂:
丝氨酸磷脂(磷脂酰丝氨酸,PS)是细胞膜的主要成分,被认为是最重要的大脑营养物质之一。PS在大脑中具有多种功能,包括支持细胞膜流动性和有益地影响神经递质系统(如乙酰胆碱、多巴胺和血清素)。长期以来,研究人员、患者及其护理人员一直对PS补充剂治疗ADHD的潜力感兴趣。2021年的一项荟萃分析发现,与安慰剂相比,每天200-300mg的PS对注意力不集中症状有显著影响48。
在2013年的一项随机对照试验中,36名被诊断为ADHD的儿童在两个月内每天服用200mg PS或安慰剂。补充PS可显著改善ADHD症状,包括注意力不集中、冲动和短期记忆;没有不良反应的报道,补充剂耐受性良好49。另一项为期15周的随机对照试验研究了PS与ω-3脂肪酸的联合作用。在这项研究中,200名患有ADHD的儿童服用了300mg PS加120mg EPA和DHA或安慰剂。该治疗显著改善了多动症症状。一项亚组分析显示,这种治疗方法对ADHD儿童尤其有效,这些儿童的多动和冲动行为更为明显。在为期15周的开放标签持续治疗中,治疗显示出持续的疗效,并且对从安慰剂切换过来的儿童有改善50。
4.乙酰L肉碱:
乙酰L肉碱(ALC)是L肉碱的一种天然衍生物,在脂肪酸代谢和细胞能量产生中发挥关键作用,也是乙酰胆碱的前体(乙酰胆碱在记忆中发挥作用)51。动物和人类研究的证据表明,它可能有助于缓解ADHD症状。在ADHD动物模型中,大鼠长期服用ALC可持续降低冲动性。这项研究还发现,冲动性动物的某些神经递质代谢产物水平发生了变化,ALC有助于改善这种不平衡52。
在一项针对112名受试者的安慰剂对照试验中,每天两次(基于体重)500–1500mg ALC改善了注意力不集中ADHD亚型儿童的症状53。在一项单独的随机双盲试验中,ALC对51名患有脆性X综合征和ADHD的男孩的多动和社交行为产生有益影响51。然而,2011年一项针对患有ADHD的女孩和男孩的研究发现,每天500–1500mg ALC与哌甲酯联合使用没有效果54。
5.茶氨酸:
L-茶氨酸是一种在茶中发现的天然化合物,已被证明有助于缓解焦虑、减轻压力和提高注意力55,56。L-茶氨碱在结构上与L-谷氨酸相似,其作用归因于其结合谷氨酸受体、抑制谷氨酸和谷氨酰胺再摄取的能力,并提高抑制性神经递质γ-氨基丁酸(GABA)的水平57。睡眠障碍是ADHD的常见合并症,也是其病因的一个因素,已证明L-茶氨酸可以改善睡眠障碍。在被诊断为ADHD的男孩(8-12岁)中,每天400mg茶氨酸被证明可以改善睡眠58。
相反,研究表明,单独使用L-茶氨酸以及与咖啡因(茶中天然存在的另一种化合物)联合使用也可以提高ADHD患者的注意力和专注力59。一项研究包括5名男性儿童(8-17岁)服用L-茶氨酸(2.5mg/kg)、咖啡因(2mg/kg)、L -茶氨酸加咖啡因或安慰剂后发现,L-茶氨酸及其组合在功能性磁共振成像(fMRI)过程中改善了认知功能,减少了精神恍惚的活动60。这些结果在一项单独的小型试验中得到证实,该试验涉及5名患有多动症的男孩(8-15岁);与安慰剂相比,服用含有L-茶氨酸和咖啡因的饮料(分别为2.5mg/kg和2mg/kg)可以改善认知功能、抑制性控制和减少走神(“白日梦”),而单独使用L-茶氨酸只能改善认知61。
6.银杏叶和人参:
银杏叶含有一种萜烯三内酯的化合物(如银杏内酯和白果内酯),对中枢神经系统有各种影响62。一项临床试验表明,银杏叶(25名患有ADHD的儿童每天服用80-120mg,持续6周)可提高教师和家长的主观评分;然而,它并没有超过哌甲酯(每天20-30mg)。在哌甲酯组中,食欲下降、头痛和失眠的副作用更常见63。
在一项为期8周的试验中,18名儿童(6-14岁)每天两次接受1000mg剂量的韩国红参;试验结束时,注意力不集中、ADHD评定量表得分和焦虑水平显著降低64。在一项初步研究中,每天服用200mg西洋参提取物和50mg银杏叶也改善了接受ADHD治疗的儿童的一系列症状,从社会问题到冲动65。
7.碧萝芷:
碧萝芷是知名的法国海松树皮提取物,具有抗氧化和血管舒张特性,在多项人类研究中已被证明有益于认知功能66。一项双盲随机试验在61名儿童中进行,为期四周,每天接受1 mg/kg碧萝芷或安慰剂治疗,4周后,碧萝芷组多动症明显减少,注意力改善,视觉和运动协调能力增强67。另一项双盲、随机、安慰剂对照试验表明,碧萝芷可降低ADHD儿童的多动和氧化应激68。
更多内容可点击其个性化综合干预方案如下:
以及参阅本网如下专文的相关内容:
医疗干预
常规治疗包括如下:
药物可以帮助控制行为和提高注意力,可能包括如下:
其他疗法
参考文献:
1. Rucklidge JJ et al. Vitamin-mineral treatment improves aggression and emotional regulation in children with ADHD: a fully blinded, randomized, placebo-controlled trial. Journal of Child Psychology and Psychiatry. 2018;59(3):232-246.
2. Darling KA et al. Mineral-Vitamin Treatment Associated with Remission in Attention-Deficit/Hyperactivity Disorder Symptoms and Related Problems: 1-Year Naturalistic Outcomes of a 10-Week Randomized Placebo-Controlled Trial. J Child Adolesc Psychopharmacol. Nov 2019;29(9):688-704.
3. Johnstone JM et al. Micronutrients for Attention-Deficit/Hyperactivity Disorder in Youths: A Placebo-Controlled Randomized Clinical Trial. J Am Acad Child Adolesc Psychiatry. May 2022;61(5):647-661.
4. Rucklidge JJ et al. Vitamin-mineral treatment of attention-deficit hyperactivity disorder in adults: double-blind randomised placebo-controlled trial. Br J Psychiatry. 2014;204:306-15.
5. Rucklidge JJ et al. Vitamin-Mineral Treatment of ADHD in Adults. Journal of attention disorders. Apr 2017;21(6):522-532.
6. Altun H et al. Homocysteine, Pyridoxine, Folate and Vitamin B12 Levels in Children with Attention Deficit Hyperactivity Disorder. Psychiatr Danub. Sep 2018;30(3):310-316.
7. Landaas ET et al. Vitamin levels in adults with ADHD. BJPsych Open. Nov 2016;2(6):377-384.
8. Rehman T et al. Cysteine and homocysteine as biomarker of various diseases. Food science & nutrition. Sep 2020;8(9):4696-4707.
9. Yektas C et al. Comparison of serum B12, folate and homocysteine concentrations in children with autism spectrum disorder or attention deficit hyperactivity disorder and healthy controls. Neuropsychiatr Dis Treat. 2019;15:2213-2219.
10. Azzini E et al. Homocysteine: Its Possible Emerging Role in At-Risk Population Groups. International journal of molecular sciences. Feb 20 2020;21(4)
11. Coleman M et al. A preliminary study of the effect of pyridoxine administration in a subgroup of hyperkinetic children: a double-blind crossover comparison with methylphenidate. Biological psychiatry. Oct 1979;14(5):741-51.
12. Kozielec T et al. Assessment of magnesium levels in children with attention deficit hyperactivity disorder (ADHD). Magnesium research : official organ of the International Society for the Development of Research on Magnesium. Jun 1997;10(2):143-8.
13. Ghanizadeh A. A systematic review of magnesium therapy for treating attention deficit hyperactivity disorder. Archives of Iranian medicine. Jul 2013;16(7):412-7.
14. Starobrat-Hermelin B et al. The effects of magnesium physiological supplementation on hyperactivity in children with attention deficit hyperactivity disorder (ADHD). Positive response to magnesium oral loading test. Magnesium research. Jun 1997;10(2):149-56.
15. Mousain-Bosc M et al. Improvement of neurobehavioral disorders in children supplemented with magnesium-vitamin B6. I. Attention deficit hyperactivity disorders. Magnesium research. Mar 2006;19(1):46-52.
16. Mousain-Bosc M et al. Magnesium VitB6 intake reduces central nervous system hyperexcitability in children. J Am Coll Nutr. Oct 2004;23(5):545s-548s.
17. Lepping P et al. Role of zinc in the pathogenesis of attention-deficit hyperactivity disorder: implications for research and treatment. CNS drugs. Sep 2010;24(9):721-8.
18. El-Bakry A et al. Zinc deficiency in children with attention-deficit hyperactivity disorder. Egyptian Journal of Psychiatry. 2019;40(2):95.
19. Akhondzadeh S et al. Zinc sulfate as an adjunct to methylphenidate for the treatment of attention deficit hyperactivity disorder in children: a double blind and randomized trial [ISRCTN64132371]. BMC psychiatry. Apr 8 2004;4:9.
20. Bilici M et al. Double-blind, placebo-controlled study of zinc sulfate in the treatment of attention deficit hyperactivity disorder. Prog Neuropsychopharmacol Biol Psychiatry. 2004 Jan;28(1):181-90.
21. Patrick LR. Restless legs syndrome: pathophysiology and the role of iron and folate. Alternative medicine review. Jun 2007;12(2):101-12.
22. Yiannikourides A et al. A Short Review of Iron Metabolism and Pathophysiology of Iron Disorders. Medicines (Basel, Switzerland). Aug 5;6(3):85.
23. Robberecht H et al. Magnesium, Iron, Zinc, Copper and Selenium Status in Attention-Deficit/Hyperactivity Disorder (ADHD). Molecules (Basel, Switzerland). Sep 27 2020;25(19)
24. Wang Y et al. Iron Status in Attention-Deficit/Hyperactivity Disorder: A Systematic Review and Meta-Analysis. PLoS One. 2017;12(1):e0169145.
25. Konofal E et al. Iron deficiency in children with attention-deficit/hyperactivity disorder. Archives of pediatrics & adolescent medicine. Dec 2004;158(12):1113-5. doi:10.1001/archpedi.158.12.1113
26. Konofal E et al. Effects of iron supplementation on attention deficit hyperactivity disorder in children. Pediatric neurology. Jan 2008;38(1):20-6.
27. Sever Y et al. Iron treatment in children with attention deficit hyperactivity disorder. A preliminary report. Neuropsychobiology. 1997;35(4):178-80.
28. Pongpitakdamrong A et al. Effect of Iron Supplementation in Children with Attention-Deficit/Hyperactivity Disorder and Iron Deficiency: A Randomized Controlled Trial. J Dev Behav Pediatr. Feb 2022, 43(2):80-86
29. Kotsi E et al. Vitamin D levels in children and adolescents with attention-deficit hyperactivity disorder (ADHD): a meta-analysis. Atten Defic Hyperact Disord. Sep 2019;11(3):221-232.
30. Khoshbakht Y et al. Vitamin D Status and Attention Deficit Hyperactivity Disorder: A Systematic Review and Meta-Analysis of Observational Studies. Adv Nutr. Jan 1 2018;9(1):9-20.
31. Silva MRM et al. Relationship between vitamin D deficiency and psychophysiological variables: a systematic review of the literature. Clinics (Sao Paulo, Brazil). 2021;76:e3155.
32. Mohammadpour N et al. Effect of vitamin D supplementation as adjunctive therapy to methylphenidate on ADHD symptoms: A randomized, double blind, placebo-controlled trial. Nutritional neuroscience. Apr 2018;21(3):202-209.
33. Dehbokri N et al. Effect of vitamin D treatment in children with attention-deficit hyperactivity disorder. World journal of pediatrics. Feb 2019;15(1):78-84.
34. Gan J et al. The Effect of Vitamin D Supplementation on Attention-Deficit/Hyperactivity Disorder: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. J Child Adolesc Psychopharmacol. Nov 2019;29(9):670-687.
35. Harding KL. Outcome-based comparison of Ritalin versus food-supplement treated children with AD/HD. Alternative medicine review. Aug 2003;8(3):319-30.
36. Colter AL et al. Fatty acid status and behavioural symptoms of attention deficit hyperactivity disorder in adolescents: a case-control study. Nutr J. Feb 14 2008;7:8. doi:10.1186/1475-2891-7-8
37. Carlson SJ et al. The role of the ω-3 fatty acid DHA in the human life cycle. JPEN Journal of parenteral and enteral nutrition. Jan 2013;37(1):15-22.
38. Patterson E et al. Health implications of high dietary omega-6 polyunsaturated Fatty acids. J Nutr Metab. 2012;2012:539426.
39. Rucklidge JJ et al. Nutrient supplementation approaches in the treatment of ADHD. Expert Rev Neurother. Apr 2009;9(4):461-76.
40. Arnold LE et al. Attention-deficit/hyperactivity disorder: dietary and nutritional treatments. Child Adolesc Psychiatr Clin N Am. Jul 2013;22(3):381-402
41. Gow RV et al. Omega-3 fatty acids are related to abnormal emotion processing in adolescent boys with attention deficit hyperactivity disorder. Prostaglandins Leukot Essent Fatty Acids. Jun 2013;88(6):419-29.
42. Gow RV et al. Omega-3 fatty acids are inversely related to callous and unemotional traits in adolescent boys with attention deficit hyperactivity disorder. Prostaglandins Leukot Essent Fatty Acids. Jun 2013;88(6):411-8.
43. Johnson M et al. Omega-3/omega-6 fatty acids for attention deficit hyperactivity disorder: a randomized placebo-controlled trial in children and adolescents. Journal of attention disorders. Mar 2009;12(5):394-401.
44. Johnson M et al. Fatty acids in ADHD: plasma profiles in a placebo-controlled study of Omega 3/6 fatty acids in children and adolescents. Atten Defic Hyperact Disord. Dec 2012;4(4):199-204.
45. Bloch MH et al. Omega-3 fatty acid supplementation for the treatment of children with attention-deficit/hyperactivity disorder symptomatology: systematic review and meta-analysis. J Am Acad Child Adolesc Psychiatry. Oct 2011;50(10):991-1000.
46. Sonuga-Barke EJ et al. Nonpharmacological interventions for ADHD: systematic review and meta-analyses of randomized controlled trials of dietary and psychological treatments. The American journal of psychiatry. Mar 2013;170(3):275-89.
47. Joshi K et al. Supplementation with flax oil and vitamin C improves the outcome of Attention Deficit Hyperactivity Disorder (ADHD). Prostaglandins Leukot Essent Fatty Acids. Jan 2006;74(1):17-21.
48. Bruton A et al. Phosphatidylserine for the Treatment of Pediatric Attention-Deficit/Hyperactivity Disorder: A Systematic Review and Meta-Analysis. Journal of alternative and complementary medicine (New York, NY). Apr 2021;27(4):312-322.
49. Hirayama S et al. The effect of phosphatidylserine administration on memory and symptoms of attention-deficit hyperactivity disorder: a randomised, double-blind, placebo-controlled clinical trial. J Hum Nutr Diet. Apr 2014;27 Suppl 2:284-91.
50. Manor I et al. The effect of phosphatidylserine containing Omega3 fatty-acids on attention-deficit hyperactivity disorder symptoms in children: a double-blind placebo-controlled trial, followed by an open-label extension. European psychiatry. Jul 2012;27(5):335-42.
51. Torrioli MG et al. A double-blind, parallel, multicenter comparison of L-acetylcarnitine with placebo on the attention deficit hyperactivity disorder in fragile X syndrome boys. Am J Med Genet A. Apr 1 2008;146a(7):803-12.
52. Adriani W et al. Acetyl-L-carnitine reduces impulsive behaviour in adolescent rats. Psychopharmacology. Nov 2004;176(3-4):296-304.
53. Arnold LE et al. Acetyl-L-carnitine (ALC) in attention-deficit/hyperactivity disorder: a multi-site, placebo-controlled pilot trial. J Child Adolesc Psychopharmacol. Dec 2007;17(6):791-802.
54. Abbasi SH et al. Acetyl-L-carnitine as an adjunctive therapy in the treatment of attention-deficit/hyperactivity disorder in children and adolescents: a placebo-controlled trial. Child Psychiatry Hum Dev. Jun 2011;42(3):367-75.
55. Williams JL et al. The Effects of Green Tea Amino Acid L-Theanine Consumption on the Ability to Manage Stress and Anxiety Levels: a Systematic Review. Plant foods for human nutrition (Dordrecht, Netherlands). Mar 2020;75(1):12-23.
56. Hidese S et al. Effects of L-Theanine Administration on Stress-Related Symptoms and Cognitive Functions in Healthy Adults: A Randomized Controlled Trial. Nutrients. Oct 3 2019;11(10)
57. Lopes Sakamoto F et al. Psychotropic effects of L-theanine and its clinical properties: From the management of anxiety and stress to a potential use in schizophrenia. Pharmacological Research. 2019/09/01/ 2019;147:104395.
58. Lyon MR et al. The effects of L-theanine (Suntheanine(R)) on objective sleep quality in boys with attention deficit hyperactivity disorder (ADHD): a randomized, double-blind, placebo-controlled clinical trial. Alternative medicine review. Dec 2011;16(4):348-54.
59. Anas Sohail A et al. The Cognitive-Enhancing Outcomes of Caffeine ancd L-theanine: A Systematic Review. Cureus. 2021;13(12)
60. Kahathuduwa C et al. L-theanine and Caffeine Improve Sustained Attention, Impulsivity and Cognition in Children with Attention Deficit Hyperactivity Disorders by Decreasing Mind Wandering (OR29-04-19). Current Developments in Nutrition. 2019;3(Supplement_1):nzz031.OR29-04-19.
61. Kahathuduwa CN et al. Effects of L-theanine-caffeine combination on sustained attention and inhibitory control among children with ADHD: a proof-of-concept neuroimaging RCT. Sci Rep. Aug 4 2020;10(1):13072.
62. Ivic L et al. Terpene trilactones from Ginkgo biloba are antagonists of cortical glycine and GABA(A) receptors. J Biol Chem. Dec 5 2003;278(49):49279-85.
63. Salehi B et al. Ginkgo biloba for attention-deficit/hyperactivity disorder in children and adolescents: a double blind, randomized controlled trial. Progress in neuro-psychopharmacology & biological psychiatry. Feb 1 2010;34(1):76-80.
64. Lee SH et al. Clinical effects of korean red ginseng on attention deficit hyperactivity disorder in children: an observational study. J Ginseng Res. Jun 2011;35(2):226-34.
65. Lyon MR et al. Effect of the herbal extract combination Panax quinquefolium and Ginkgo biloba on attention-deficit hyperactivity disorder: a pilot study. Journal of psychiatry & neuroscience. May 2001;26(3):221-8.
66. Simpson T et al. Assessing the Efficacy and Mechanisms of Pycnogenol(®) on Cognitive Aging From In Vitro Animal and Human Studies. Frontiers in pharmacology. 2019;10:694.
67. Trebatická J et al. Treatment of ADHD with French maritime pine bark extract, Pycnogenol. European child & adolescent psychiatry. Sep 2006;15(6):329-35.
68. Dvoráková M et al. Urinary catecholamines in children with attention deficit hyperactivity disorder (ADHD): modulation by a polyphenolic extract from pine bark (pycnogenol). Nutritional neuroscience. Jun-Aug 2007;10(3-4):151-7.
美国注意力缺陷障碍协会
http://www.add.org
美国梅奥诊所
www.mayoclinic.org
美国儿童和成人多动症和注意力缺陷网
http://www.chadd.org
美国国立卫生研究院公众健康网
www.medlineplus.gov
加拿大关于儿童健康网
http://www.aboutkidshealth.ca
加拿大精神病学协会
http://www.cpa-apc.org
免责声明和安全信息
英文名称:Attention Deficit Hyperactivity Disorder and Attention Deficit Disorder,ADHD and ADD; Hyperkinetic Syndrome; Hyperkinetic Impulse Disorder
定义
注意缺陷多动障碍(ADHD)是一种疾病,影响人的行为。它可引起多动、冲动的行为和/或难以集中注意力。这些行为问题可持续超过一段很长的时间。多动症可以影响所有年龄的人。ADHD有3种类型:
- 注意力缺陷障碍(ADD)
- 多动冲动障碍
- 二者结合:注意缺陷多动障碍(ADHD),是最常见的类型
病因
ADHD的病因是未知的。研究者相信它是由若干因素相互作用引起的,最有可能是导致大脑中的化学物质不平衡。但在大脑发育过程中,变化可能发生。此外,遗传基因和环境因素都可能发挥了作用。风险因素
以下因素可增加ADHD的几率,包括:- 早产
- 父母或兄弟姐妹(特别是同卵双胞胎)患ADHD
- 母亲抽烟、喝酒,有尿路感染,或早产
- 父母有健康状况,如酒精滥用和转换障碍
- 颅脑损伤,在2岁前
- 睡眠障碍,如睡眠呼吸暂停
- 接触铅或某些杀虫剂
症状
成人ADHD可导致社会关系、工作绩效、工作去留等问题。症状根据ADHD的类型而不同:
- 注意力缺陷障碍,如:
- 容易分心
- 不注意细节
- 不细心听讲
- 犯粗心的错误
- 不遵从指示或任务
- 躲避或不喜欢需要长时间努力的活动
- 丢失或忘记为完成必要任务的东西
- 经常忘记日常的活动
- 多动冲动障碍,如:
- 坐立不安、手、脚烦躁不安和难为情
- 不停地跑和爬、不能安静坐着
- 脱口而出答案,在未听到完整的问题之前
- 难以安静地玩
- 说话过多
- 打断别人说话
- 等待或排队没耐心
- ADHD表现为上述二者症状的组合。
- 抑郁症
- 焦虑症
- 情绪障碍
- 癫痫
- 品行障碍,难于遵守社会规则
- 对立违抗性障碍:负面,愤怒和挑衅行为
- 学习和语言障碍
- 身体条件,如睡眠呼吸暂停症
- 睡眠问题
- 物质滥用,如酒精、咖啡因和药物等
- 吸烟
疗法
综合选项可包括如下:调整饮食与生活方式
越来越多的研究表明饮食变化可以显着改善ADHD症状:
- 避免高糖食物,因为可能引起多动
- 早餐营养丰富、全面
- 经常锻炼、户外活动
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控ADHD的营养和草本补充剂,主要包括如下:
1.维生素和矿物质类:
1.1.复合维矿素等多种营养素:
- 儿童研究:含有维生素、矿物质和氨基酸的综合营养补充剂可能有助于改善ADHD的症状。在一项完全盲法对照试验中1,93名患有ADHD的儿童(7-12岁)没有服用任何药物,受试者被随机分配接受提供微量营养素(13种维生素,17种矿物质和4种氨基酸)的营养补充剂或安慰剂,为期10周。配方中的大多数营养素的剂量在建议的每日摄入量(RDA)和传统上可耐受的上限摄入量(UL)之间。临床整体印象改善量表(CGI-I,衡量临床医生对患者整体功能的看法)有显著改善,其中47%的接受微量营养素组被确定为改善,而安慰剂患者为28%。此外,32%服用微量营养素的受试者在注意力方面表现出临床意义上的改善,而安慰剂组只有9%。临床医生、家长和教师的报告还发现,与安慰剂相比,服用微量营养素的儿童在情绪调节、攻击性和一般功能方面表现出更大的改善1。在该试验的一年随访中,短期受益于微量营养素儿童在随访中保持了这些改善,没有副作用。84%的仍在服用微量营养素的参与者被确定为相对于基线而言整体功能有所改善,相比之下,50%的参与者转向精神药物,21%的参与者停止治疗,这有力地支持了补充微量营养素在改善ADHD症状中的作用2。
- 青少年研究:在青少年多动症微量营养素(MADDY)研究中,135名6-12岁的非药物儿童被随机分配接受提供36种微量营养素(维生素、矿物质、氨基酸和抗氧化剂)的营养补充剂或安慰剂治疗8周。在CGI-I量表上,与安慰剂组的18%相比,54%的微量营养素组表现出改善;然而,父母报告的两组的改善情况相似3。
- 成人研究:含有微量营养素的营养补充剂对成人ADHD的影响也得到了评估。在一项双盲对照试验中4,80名成年人随机接受广谱多种维生素/矿物质和植物配方或安慰剂治疗8周,与安慰剂相比,服用微量营养素的人多动症症状有所改善。根据总体功能评估量表(GAF)的测量,微量营养素组显示出更大的整体改善,64.3%的微量营养素小组参与者在康纳斯成人ADHD评定量表(CAARS)的至少一个亚量表上显示出≥30%的下降,该量表用于评估多动症的各种症状,如注意力不集中、记忆问题和多动,而安慰剂组为36.8%。与安慰剂相比,微量营养素组中更多的参与者在CGI-I量表上也被评为有所改善4。对其中72名受试者进行的一年随访发现,那些继续服用微量营养素的受试者仍比最初的基线有显著改善,并且表现比那些改用精神药物或停止微量营养素治疗的受试人更好5。
1.2.维生素B族:
B族维生素是一类水溶性营养素,在新陈代谢和维持体内平衡方面发挥着至关重要的作用。已发现患有ADHD儿童和成人的B族维生素,即维生素B6(吡哆醇)和叶酸(B9)水平降低;此外,发现患有多动症的儿童的维生素B12(钴胺素)水平显著低于对照组6,7,。B族维生素缺乏可能会导致疾病病理,因为它们在血清素、儿茶酚胺和其他单胺类的产生中起着重要作用。
B族维生素也因其降低血液同型半胱氨酸水平的能力而备受关注,因为在包括ADHD在内的多种疾病中都观察到高水平的同型半胱氨酸,并可能导致氧化应激8-10。需要进一步的研究来阐明B族维生素和同型半胱氨酸在ADHD病理中的关系。
1.3.维生素B6和镁:
维生素B6(吡哆醇)与血清素的产生有关。早期研究发现,补充B6可以提高血清素水平,改善ADHD的多动症状11。在一项营养调查中,将100名ADHD患者与150名健康人进行了比较,发现ADHD患者的维生素B6摄入水平明显较低。研究还表明,镁缺乏症在多动症患者中很常见12,13。在一项安慰剂对照试验中,每天补充约200mg镁,持续六个月,显示7-12岁ADHD儿童的多动症状显著减少14。
一项针对40名ADHD儿童的为期8周的研究发现,补充镁(6mg/kg/天)和维生素B6(0.6mg/kg/天)可以改善多动症和学校注意力。有趣的是,当停止治疗方案时,儿童的症状在几周内再次出现15。在同一研究人员之前的一项研究中,类似的维生素B6和镁补充剂方案改善了过度兴奋症状。在这项研究中,52名过度兴奋的儿童服用了镁-B6补充剂,为期6个月;在治疗期间,所有受试者的身体攻击性和注意力等症状都有所改善16。
1.4.锌:
锌参与多巴胺能信号传导,已被证明是ADHD患者常见的营养缺乏症17,18。与接受利他林和安慰剂治疗的儿童相比,接受利他林治疗六周的多动症儿童在同时服用锌补充剂(每天55mg硫酸锌,提供15mg元素锌)时,从老师和家长那里获得了更好的行为评价19。
在一项针对400名ADHD儿童(平均年龄9.6岁)的大型研究中,作为单一疗法,每天150mg硫酸锌持续12周,与安慰剂相比,可显著改善多动、冲动和社交障碍症状20。
1.5.铁:
铁是身体中的一种重要微量元素,对生长、发育、红细胞氧气输送和多巴胺信号传导很重要21。铁以铁蛋白储存在体内,铁蛋白随后可以按照身体的要求以可控的方式释放铁22。在ADHD患者中观察到低铁蛋白水平,提示铁蛋白在多动症病理中的重要作用23,24。许多患有多动症的儿童都是缺铁性的,缺铁的严重程度与症状的严重程度相关25。在患有ADHD和睡眠障碍(如不安腿综合征)的儿童中也观察到低铁水平23,21。
一项针对23名患有ADHD和缺铁(定义为铁蛋白水平低于30ng/mL)的儿童(5-8岁)的随机安慰剂对照研究表明,在12周内每天补充80mg硫酸亚铁(提供16mg元素铁)可显著降低症状26。另一项针对14名受试者(7-11岁)的试验表明,每天补充5mg/kg持续30天,显著降低了父母对ADHD症状的评分27。在一项对52名服用哌甲酯的缺铁儿童进行的试验中,随机接受补铁(含80mg元素铁的300mg硫酸亚铁胶囊)或安慰剂12周,父母报告接受铁治疗的儿童ADHD症状有显著改善,但接受安慰剂治疗的人则没有28。
需要注意的是,超过膳食推荐量(RDA)的高剂量铁(如这些试验中使用的铁)只能在医疗从业者的指导下使用,因为意外过量服用含铁产品是6岁以下儿童致命中毒的主要原因。
1.6.维生素D:
维生素D是一种脂溶性维生素,通过饮食获得,并由身体在阳光照射下合成。维生素D缺乏被认为是几种神经精神障碍的可能原因,也可能是ADHD的危险因素。一项对8项共11,324名儿童(2655名患有多动症)的研究进行的荟萃分析发现,与健康对照组相比,被诊断为ADHD
的患者的维生素D血清水平显著较低29。在一项对5项研究进行的另一项荟萃分析中,维生素D状态较低与患ADHD的风险较高显著相关30。维生素D缺乏也可能导致情绪障碍,通常与ADHD共存31。
补充维生素D已在各种临床试验中被用作改善ADHD症状的治疗方法。一项双盲试验将54名儿童(5-12岁)随机分组,接受2000 IU(50mcg)维生素D或安慰剂治疗8周,作为哌甲酯的辅助治疗。虽然ADHD症状在两组中均显著降低,每周通过父母晚间和早晨行为评分(WPREMB)标准化评估观察到的晚间症状,在服用维生素D的第4周和第8周得到改善32。在一项单独的试验中,包括96名患有ADHD的儿童,随机接受每周50,000 IU(1250mcg)的维生素D或安慰剂治疗六周(以及稳定的每日剂量的哌甲酯),维生素D组的多动症症状有所改善,对注意力不集中症状有特别的影响33。此外,一项包含256名儿童的四项随机对照试验的系统回顾和荟萃分析发现,维生素D补充剂在ADHD总分、注意力不集中评分、多动评分和行为评分方面显示出虽小但在统计学上显著的改善34。
一项医院研究实例:ADHD管理的多种营养配方
ADHD的多因素起源表明,针对多种特定潜在促成因素的干预可能是有益的。为了验证这一假设,美国马萨诸塞州McLean医院的研究人员将20名患有ADHD的儿童分为两组。一组10名儿童每天服用5-15mg利他林2-3次,另一组接受综合性多营养配方,该配方旨在针对可能在ADHD发展中发挥作用的几个因素35。
本研究中使用的多种营养配方包括益生菌、氨基酸(如酪氨酸、组氨酸、谷氨酰胺、甘氨酸、蛋氨酸和半胱氨酸)、必需脂肪酸和磷脂(如EPA、DHA和磷脂酰胆碱)以及维生素和矿物质。
令人印象深刻的是,在标准化ADHD评估中,服用多种营养配方的儿童在4周时的ADHD症状改善程度与服用利他林的儿童相同。在结束研究时,研究人员指出:“两组的进步……都是显著的,基本上是相同的……”
2.必需脂肪酸:
研究发现,患有ADHD的儿童血液中的ω-3脂肪酸水平可能较低36。虽然现代饮食通常含有过多的某些ω-6脂肪酸,但缺乏ω-3脂肪酸类(包括EPA和DHA)37,38。考虑到产生多巴胺的神经末梢由高达80%的ω-3脂酸DHA组成39,这些分子在中枢神经系统及其功能中具有重要作用。在儿童中,ADHD症状的严重程度与较低水平的ω-3和较高水平的ω-6脂肪酸有关。一般来说,多动和注意力不集中也与ω-3脂肪酸缺乏有关,因此表明这可能是ADHD的一个风险因素40。
英国一项针对493名7-9岁学龄儿童的研究发现,ω-3脂肪酸缺乏非常常见,并与ADHD相关症状(如对立行为和情绪不稳定)有关。另一组研究发现,血液中ω-3脂肪酸水平低与冷酷无情的行为、反社会特征和情绪处理受损有关41,42。
瑞典科学家研究了鱼油补充剂对75名患有多动症的儿童和青少年的影响,这些鱼油补充剂含有ω-3脂肪酸(每天558mg EPA, 174mg DHA)和有益的ω-6脂肪酸亚麻酸GLA(60mg/天)。他们发现,六个月后,近一半的受试者对ω-3和ω-6补充剂有反应,ADHD症状减轻43。在随后对这些研究数据的分析中,同样的研究人员发现,症状减轻至少25%的受试者在三个月和六个月时,血液中ω-6与ω-3的比例显著降低44。
耶鲁大学研究人员进行的一项全面审查,回顾了涉及699名ADHD儿童的10项试验的证据。研究发现,补充ω-3脂肪酸可以适度改善研究参与者的ADHD症状。研究人员在总结中指出,“……使用ω-3脂肪补充剂来加强传统的药物干预可能是合理的……”45。对几项已发表研究的分析还发现,补充游离脂肪酸和从饮食中排除人工食用色素,在减少ADHD症状方面具有统计学上的显著效果46。
亚麻籽油提供高水平的ω-3脂肪酸α-亚麻酸(ALA),这是EPA和DHA的前体,也可能有益。一项研究考察了每天两次给患有ADHD的儿童补充亚麻油乳剂(提供200mg ALA)和维生素C乳剂(25mg)的益处,发现ADHD的症状显著改善,包括冲动、烦躁、注意力不集中和自我控制,这反映在多动症总分的降低上47。
鱼油是多不饱和ω-3脂肪酸的良好来源。脂肪酸水平的平衡可以通过血液测试来测量,服用脂肪酸补充剂的人可以重复进行血液测试来衡量其效果。
3.丝氨酸磷脂:
丝氨酸磷脂(磷脂酰丝氨酸,PS)是细胞膜的主要成分,被认为是最重要的大脑营养物质之一。PS在大脑中具有多种功能,包括支持细胞膜流动性和有益地影响神经递质系统(如乙酰胆碱、多巴胺和血清素)。长期以来,研究人员、患者及其护理人员一直对PS补充剂治疗ADHD的潜力感兴趣。2021年的一项荟萃分析发现,与安慰剂相比,每天200-300mg的PS对注意力不集中症状有显著影响48。
在2013年的一项随机对照试验中,36名被诊断为ADHD的儿童在两个月内每天服用200mg PS或安慰剂。补充PS可显著改善ADHD症状,包括注意力不集中、冲动和短期记忆;没有不良反应的报道,补充剂耐受性良好49。另一项为期15周的随机对照试验研究了PS与ω-3脂肪酸的联合作用。在这项研究中,200名患有ADHD的儿童服用了300mg PS加120mg EPA和DHA或安慰剂。该治疗显著改善了多动症症状。一项亚组分析显示,这种治疗方法对ADHD儿童尤其有效,这些儿童的多动和冲动行为更为明显。在为期15周的开放标签持续治疗中,治疗显示出持续的疗效,并且对从安慰剂切换过来的儿童有改善50。
4.乙酰L肉碱:
乙酰L肉碱(ALC)是L肉碱的一种天然衍生物,在脂肪酸代谢和细胞能量产生中发挥关键作用,也是乙酰胆碱的前体(乙酰胆碱在记忆中发挥作用)51。动物和人类研究的证据表明,它可能有助于缓解ADHD症状。在ADHD动物模型中,大鼠长期服用ALC可持续降低冲动性。这项研究还发现,冲动性动物的某些神经递质代谢产物水平发生了变化,ALC有助于改善这种不平衡52。
在一项针对112名受试者的安慰剂对照试验中,每天两次(基于体重)500–1500mg ALC改善了注意力不集中ADHD亚型儿童的症状53。在一项单独的随机双盲试验中,ALC对51名患有脆性X综合征和ADHD的男孩的多动和社交行为产生有益影响51。然而,2011年一项针对患有ADHD的女孩和男孩的研究发现,每天500–1500mg ALC与哌甲酯联合使用没有效果54。
5.茶氨酸:
L-茶氨酸是一种在茶中发现的天然化合物,已被证明有助于缓解焦虑、减轻压力和提高注意力55,56。L-茶氨碱在结构上与L-谷氨酸相似,其作用归因于其结合谷氨酸受体、抑制谷氨酸和谷氨酰胺再摄取的能力,并提高抑制性神经递质γ-氨基丁酸(GABA)的水平57。睡眠障碍是ADHD的常见合并症,也是其病因的一个因素,已证明L-茶氨酸可以改善睡眠障碍。在被诊断为ADHD的男孩(8-12岁)中,每天400mg茶氨酸被证明可以改善睡眠58。
相反,研究表明,单独使用L-茶氨酸以及与咖啡因(茶中天然存在的另一种化合物)联合使用也可以提高ADHD患者的注意力和专注力59。一项研究包括5名男性儿童(8-17岁)服用L-茶氨酸(2.5mg/kg)、咖啡因(2mg/kg)、L -茶氨酸加咖啡因或安慰剂后发现,L-茶氨酸及其组合在功能性磁共振成像(fMRI)过程中改善了认知功能,减少了精神恍惚的活动60。这些结果在一项单独的小型试验中得到证实,该试验涉及5名患有多动症的男孩(8-15岁);与安慰剂相比,服用含有L-茶氨酸和咖啡因的饮料(分别为2.5mg/kg和2mg/kg)可以改善认知功能、抑制性控制和减少走神(“白日梦”),而单独使用L-茶氨酸只能改善认知61。
6.银杏叶和人参:
银杏叶含有一种萜烯三内酯的化合物(如银杏内酯和白果内酯),对中枢神经系统有各种影响62。一项临床试验表明,银杏叶(25名患有ADHD的儿童每天服用80-120mg,持续6周)可提高教师和家长的主观评分;然而,它并没有超过哌甲酯(每天20-30mg)。在哌甲酯组中,食欲下降、头痛和失眠的副作用更常见63。
在一项为期8周的试验中,18名儿童(6-14岁)每天两次接受1000mg剂量的韩国红参;试验结束时,注意力不集中、ADHD评定量表得分和焦虑水平显著降低64。在一项初步研究中,每天服用200mg西洋参提取物和50mg银杏叶也改善了接受ADHD治疗的儿童的一系列症状,从社会问题到冲动65。
7.碧萝芷:
碧萝芷是知名的法国海松树皮提取物,具有抗氧化和血管舒张特性,在多项人类研究中已被证明有益于认知功能66。一项双盲随机试验在61名儿童中进行,为期四周,每天接受1 mg/kg碧萝芷或安慰剂治疗,4周后,碧萝芷组多动症明显减少,注意力改善,视觉和运动协调能力增强67。另一项双盲、随机、安慰剂对照试验表明,碧萝芷可降低ADHD儿童的多动和氧化应激68。
更多内容可点击其个性化综合干预方案如下:
以及参阅本网如下专文的相关内容:
医疗干预
常规治疗包括如下:
药物可以帮助控制行为和提高注意力,可能包括如下:
- 选择性去甲肾上腺素再摄取抑制剂:提高注意力和减少冲动和多动
- 抗抑郁药物:管理抑郁症状
- 抗精神病药物:治疗攻击性行为
- α激动剂降压药物:治疗冲动
其他疗法
- 行为疗法:服用药物并接受行为疗法,要比单纯使用药物治疗效果更佳。
- 治疗专注于社会实践和解决问题的能力。
- 辅导员会教给父母和老师的技术以帮助那些患者,这可能包括在课堂上的变化,以及父母教养方式。例如,在学校教室的座椅上放置一个充气坐垫,可以延长他们集中注意力的时间。
- ADHD训练法也有益。教练与患者协作,帮助他们组织和创新策略,以提高效率和成功。
- 良好睡眠:没有足够的睡眠可能会遭受严重的行为问题。治疗的关键是确保缓则得到充足的睡眠。
预防
因为ADHD确切病因未明,没有预防指南。参考文献:
1. Rucklidge JJ et al. Vitamin-mineral treatment improves aggression and emotional regulation in children with ADHD: a fully blinded, randomized, placebo-controlled trial. Journal of Child Psychology and Psychiatry. 2018;59(3):232-246.
2. Darling KA et al. Mineral-Vitamin Treatment Associated with Remission in Attention-Deficit/Hyperactivity Disorder Symptoms and Related Problems: 1-Year Naturalistic Outcomes of a 10-Week Randomized Placebo-Controlled Trial. J Child Adolesc Psychopharmacol. Nov 2019;29(9):688-704.
3. Johnstone JM et al. Micronutrients for Attention-Deficit/Hyperactivity Disorder in Youths: A Placebo-Controlled Randomized Clinical Trial. J Am Acad Child Adolesc Psychiatry. May 2022;61(5):647-661.
4. Rucklidge JJ et al. Vitamin-mineral treatment of attention-deficit hyperactivity disorder in adults: double-blind randomised placebo-controlled trial. Br J Psychiatry. 2014;204:306-15.
5. Rucklidge JJ et al. Vitamin-Mineral Treatment of ADHD in Adults. Journal of attention disorders. Apr 2017;21(6):522-532.
6. Altun H et al. Homocysteine, Pyridoxine, Folate and Vitamin B12 Levels in Children with Attention Deficit Hyperactivity Disorder. Psychiatr Danub. Sep 2018;30(3):310-316.
7. Landaas ET et al. Vitamin levels in adults with ADHD. BJPsych Open. Nov 2016;2(6):377-384.
8. Rehman T et al. Cysteine and homocysteine as biomarker of various diseases. Food science & nutrition. Sep 2020;8(9):4696-4707.
9. Yektas C et al. Comparison of serum B12, folate and homocysteine concentrations in children with autism spectrum disorder or attention deficit hyperactivity disorder and healthy controls. Neuropsychiatr Dis Treat. 2019;15:2213-2219.
10. Azzini E et al. Homocysteine: Its Possible Emerging Role in At-Risk Population Groups. International journal of molecular sciences. Feb 20 2020;21(4)
11. Coleman M et al. A preliminary study of the effect of pyridoxine administration in a subgroup of hyperkinetic children: a double-blind crossover comparison with methylphenidate. Biological psychiatry. Oct 1979;14(5):741-51.
12. Kozielec T et al. Assessment of magnesium levels in children with attention deficit hyperactivity disorder (ADHD). Magnesium research : official organ of the International Society for the Development of Research on Magnesium. Jun 1997;10(2):143-8.
13. Ghanizadeh A. A systematic review of magnesium therapy for treating attention deficit hyperactivity disorder. Archives of Iranian medicine. Jul 2013;16(7):412-7.
14. Starobrat-Hermelin B et al. The effects of magnesium physiological supplementation on hyperactivity in children with attention deficit hyperactivity disorder (ADHD). Positive response to magnesium oral loading test. Magnesium research. Jun 1997;10(2):149-56.
15. Mousain-Bosc M et al. Improvement of neurobehavioral disorders in children supplemented with magnesium-vitamin B6. I. Attention deficit hyperactivity disorders. Magnesium research. Mar 2006;19(1):46-52.
16. Mousain-Bosc M et al. Magnesium VitB6 intake reduces central nervous system hyperexcitability in children. J Am Coll Nutr. Oct 2004;23(5):545s-548s.
17. Lepping P et al. Role of zinc in the pathogenesis of attention-deficit hyperactivity disorder: implications for research and treatment. CNS drugs. Sep 2010;24(9):721-8.
18. El-Bakry A et al. Zinc deficiency in children with attention-deficit hyperactivity disorder. Egyptian Journal of Psychiatry. 2019;40(2):95.
19. Akhondzadeh S et al. Zinc sulfate as an adjunct to methylphenidate for the treatment of attention deficit hyperactivity disorder in children: a double blind and randomized trial [ISRCTN64132371]. BMC psychiatry. Apr 8 2004;4:9.
20. Bilici M et al. Double-blind, placebo-controlled study of zinc sulfate in the treatment of attention deficit hyperactivity disorder. Prog Neuropsychopharmacol Biol Psychiatry. 2004 Jan;28(1):181-90.
21. Patrick LR. Restless legs syndrome: pathophysiology and the role of iron and folate. Alternative medicine review. Jun 2007;12(2):101-12.
22. Yiannikourides A et al. A Short Review of Iron Metabolism and Pathophysiology of Iron Disorders. Medicines (Basel, Switzerland). Aug 5;6(3):85.
23. Robberecht H et al. Magnesium, Iron, Zinc, Copper and Selenium Status in Attention-Deficit/Hyperactivity Disorder (ADHD). Molecules (Basel, Switzerland). Sep 27 2020;25(19)
24. Wang Y et al. Iron Status in Attention-Deficit/Hyperactivity Disorder: A Systematic Review and Meta-Analysis. PLoS One. 2017;12(1):e0169145.
25. Konofal E et al. Iron deficiency in children with attention-deficit/hyperactivity disorder. Archives of pediatrics & adolescent medicine. Dec 2004;158(12):1113-5. doi:10.1001/archpedi.158.12.1113
26. Konofal E et al. Effects of iron supplementation on attention deficit hyperactivity disorder in children. Pediatric neurology. Jan 2008;38(1):20-6.
27. Sever Y et al. Iron treatment in children with attention deficit hyperactivity disorder. A preliminary report. Neuropsychobiology. 1997;35(4):178-80.
28. Pongpitakdamrong A et al. Effect of Iron Supplementation in Children with Attention-Deficit/Hyperactivity Disorder and Iron Deficiency: A Randomized Controlled Trial. J Dev Behav Pediatr. Feb 2022, 43(2):80-86
29. Kotsi E et al. Vitamin D levels in children and adolescents with attention-deficit hyperactivity disorder (ADHD): a meta-analysis. Atten Defic Hyperact Disord. Sep 2019;11(3):221-232.
30. Khoshbakht Y et al. Vitamin D Status and Attention Deficit Hyperactivity Disorder: A Systematic Review and Meta-Analysis of Observational Studies. Adv Nutr. Jan 1 2018;9(1):9-20.
31. Silva MRM et al. Relationship between vitamin D deficiency and psychophysiological variables: a systematic review of the literature. Clinics (Sao Paulo, Brazil). 2021;76:e3155.
32. Mohammadpour N et al. Effect of vitamin D supplementation as adjunctive therapy to methylphenidate on ADHD symptoms: A randomized, double blind, placebo-controlled trial. Nutritional neuroscience. Apr 2018;21(3):202-209.
33. Dehbokri N et al. Effect of vitamin D treatment in children with attention-deficit hyperactivity disorder. World journal of pediatrics. Feb 2019;15(1):78-84.
34. Gan J et al. The Effect of Vitamin D Supplementation on Attention-Deficit/Hyperactivity Disorder: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. J Child Adolesc Psychopharmacol. Nov 2019;29(9):670-687.
35. Harding KL. Outcome-based comparison of Ritalin versus food-supplement treated children with AD/HD. Alternative medicine review. Aug 2003;8(3):319-30.
36. Colter AL et al. Fatty acid status and behavioural symptoms of attention deficit hyperactivity disorder in adolescents: a case-control study. Nutr J. Feb 14 2008;7:8. doi:10.1186/1475-2891-7-8
37. Carlson SJ et al. The role of the ω-3 fatty acid DHA in the human life cycle. JPEN Journal of parenteral and enteral nutrition. Jan 2013;37(1):15-22.
38. Patterson E et al. Health implications of high dietary omega-6 polyunsaturated Fatty acids. J Nutr Metab. 2012;2012:539426.
39. Rucklidge JJ et al. Nutrient supplementation approaches in the treatment of ADHD. Expert Rev Neurother. Apr 2009;9(4):461-76.
40. Arnold LE et al. Attention-deficit/hyperactivity disorder: dietary and nutritional treatments. Child Adolesc Psychiatr Clin N Am. Jul 2013;22(3):381-402
41. Gow RV et al. Omega-3 fatty acids are related to abnormal emotion processing in adolescent boys with attention deficit hyperactivity disorder. Prostaglandins Leukot Essent Fatty Acids. Jun 2013;88(6):419-29.
42. Gow RV et al. Omega-3 fatty acids are inversely related to callous and unemotional traits in adolescent boys with attention deficit hyperactivity disorder. Prostaglandins Leukot Essent Fatty Acids. Jun 2013;88(6):411-8.
43. Johnson M et al. Omega-3/omega-6 fatty acids for attention deficit hyperactivity disorder: a randomized placebo-controlled trial in children and adolescents. Journal of attention disorders. Mar 2009;12(5):394-401.
44. Johnson M et al. Fatty acids in ADHD: plasma profiles in a placebo-controlled study of Omega 3/6 fatty acids in children and adolescents. Atten Defic Hyperact Disord. Dec 2012;4(4):199-204.
45. Bloch MH et al. Omega-3 fatty acid supplementation for the treatment of children with attention-deficit/hyperactivity disorder symptomatology: systematic review and meta-analysis. J Am Acad Child Adolesc Psychiatry. Oct 2011;50(10):991-1000.
46. Sonuga-Barke EJ et al. Nonpharmacological interventions for ADHD: systematic review and meta-analyses of randomized controlled trials of dietary and psychological treatments. The American journal of psychiatry. Mar 2013;170(3):275-89.
47. Joshi K et al. Supplementation with flax oil and vitamin C improves the outcome of Attention Deficit Hyperactivity Disorder (ADHD). Prostaglandins Leukot Essent Fatty Acids. Jan 2006;74(1):17-21.
48. Bruton A et al. Phosphatidylserine for the Treatment of Pediatric Attention-Deficit/Hyperactivity Disorder: A Systematic Review and Meta-Analysis. Journal of alternative and complementary medicine (New York, NY). Apr 2021;27(4):312-322.
49. Hirayama S et al. The effect of phosphatidylserine administration on memory and symptoms of attention-deficit hyperactivity disorder: a randomised, double-blind, placebo-controlled clinical trial. J Hum Nutr Diet. Apr 2014;27 Suppl 2:284-91.
50. Manor I et al. The effect of phosphatidylserine containing Omega3 fatty-acids on attention-deficit hyperactivity disorder symptoms in children: a double-blind placebo-controlled trial, followed by an open-label extension. European psychiatry. Jul 2012;27(5):335-42.
51. Torrioli MG et al. A double-blind, parallel, multicenter comparison of L-acetylcarnitine with placebo on the attention deficit hyperactivity disorder in fragile X syndrome boys. Am J Med Genet A. Apr 1 2008;146a(7):803-12.
52. Adriani W et al. Acetyl-L-carnitine reduces impulsive behaviour in adolescent rats. Psychopharmacology. Nov 2004;176(3-4):296-304.
53. Arnold LE et al. Acetyl-L-carnitine (ALC) in attention-deficit/hyperactivity disorder: a multi-site, placebo-controlled pilot trial. J Child Adolesc Psychopharmacol. Dec 2007;17(6):791-802.
54. Abbasi SH et al. Acetyl-L-carnitine as an adjunctive therapy in the treatment of attention-deficit/hyperactivity disorder in children and adolescents: a placebo-controlled trial. Child Psychiatry Hum Dev. Jun 2011;42(3):367-75.
55. Williams JL et al. The Effects of Green Tea Amino Acid L-Theanine Consumption on the Ability to Manage Stress and Anxiety Levels: a Systematic Review. Plant foods for human nutrition (Dordrecht, Netherlands). Mar 2020;75(1):12-23.
56. Hidese S et al. Effects of L-Theanine Administration on Stress-Related Symptoms and Cognitive Functions in Healthy Adults: A Randomized Controlled Trial. Nutrients. Oct 3 2019;11(10)
57. Lopes Sakamoto F et al. Psychotropic effects of L-theanine and its clinical properties: From the management of anxiety and stress to a potential use in schizophrenia. Pharmacological Research. 2019/09/01/ 2019;147:104395.
58. Lyon MR et al. The effects of L-theanine (Suntheanine(R)) on objective sleep quality in boys with attention deficit hyperactivity disorder (ADHD): a randomized, double-blind, placebo-controlled clinical trial. Alternative medicine review. Dec 2011;16(4):348-54.
59. Anas Sohail A et al. The Cognitive-Enhancing Outcomes of Caffeine ancd L-theanine: A Systematic Review. Cureus. 2021;13(12)
60. Kahathuduwa C et al. L-theanine and Caffeine Improve Sustained Attention, Impulsivity and Cognition in Children with Attention Deficit Hyperactivity Disorders by Decreasing Mind Wandering (OR29-04-19). Current Developments in Nutrition. 2019;3(Supplement_1):nzz031.OR29-04-19.
61. Kahathuduwa CN et al. Effects of L-theanine-caffeine combination on sustained attention and inhibitory control among children with ADHD: a proof-of-concept neuroimaging RCT. Sci Rep. Aug 4 2020;10(1):13072.
62. Ivic L et al. Terpene trilactones from Ginkgo biloba are antagonists of cortical glycine and GABA(A) receptors. J Biol Chem. Dec 5 2003;278(49):49279-85.
63. Salehi B et al. Ginkgo biloba for attention-deficit/hyperactivity disorder in children and adolescents: a double blind, randomized controlled trial. Progress in neuro-psychopharmacology & biological psychiatry. Feb 1 2010;34(1):76-80.
64. Lee SH et al. Clinical effects of korean red ginseng on attention deficit hyperactivity disorder in children: an observational study. J Ginseng Res. Jun 2011;35(2):226-34.
65. Lyon MR et al. Effect of the herbal extract combination Panax quinquefolium and Ginkgo biloba on attention-deficit hyperactivity disorder: a pilot study. Journal of psychiatry & neuroscience. May 2001;26(3):221-8.
66. Simpson T et al. Assessing the Efficacy and Mechanisms of Pycnogenol(®) on Cognitive Aging From In Vitro Animal and Human Studies. Frontiers in pharmacology. 2019;10:694.
67. Trebatická J et al. Treatment of ADHD with French maritime pine bark extract, Pycnogenol. European child & adolescent psychiatry. Sep 2006;15(6):329-35.
68. Dvoráková M et al. Urinary catecholamines in children with attention deficit hyperactivity disorder (ADHD): modulation by a polyphenolic extract from pine bark (pycnogenol). Nutritional neuroscience. Jun-Aug 2007;10(3-4):151-7.
参考来源:
美国注意力缺陷障碍协会
http://www.add.org
美国梅奥诊所
www.mayoclinic.org
美国儿童和成人多动症和注意力缺陷网
http://www.chadd.org
美国国立卫生研究院公众健康网
www.medlineplus.gov
加拿大关于儿童健康网
http://www.aboutkidshealth.ca
加拿大精神病学协会
http://www.cpa-apc.org
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

